近日,云南大学、云南农业大学与中国地质大学(武汉)等科研单位首次系统揭示了磷富集对淡水湖泊微生物群落、病毒群落及其代谢功能的影响,为理解富营养化背景下病毒生态功能提供了全新视角。研究结果以“Phosphorus Enrichment Rewires Viral-Mediated Biogeochemical Processes in Freshwater Ecosystems”为题在线发表于国际期刊Journal of Earth Science(中科院1区TOP,IF 4.7)。

磷是生命必需元素,但过量输入会引发水体富营养化,导致蓝藻暴发、溶解氧下降、生态系统退化。尽管磷对细菌群落的影响已有大量研究,但病毒如何响应磷富营养化、是否参与磷循环调控,一直缺乏系统性认识。研究团队在云南抚仙湖开展微观生态实验,通过添加磷酸盐模拟磷富营养化过程,结合16S rRNA基因扩增测序、病毒宏基因组学、代谢功能预测等多种手段,分析了56天内微生物与病毒群落的动态变化。同时,解析了磷富集条件下,病毒群落在磷代谢过程中的重要生态功能。
研究发现磷添加促进了蓝藻等富营养型微生物的增殖,影响微生物磷代谢过程,改变微生物间互作网络,降低群落稳定性,导致水体中微生物群落重组。
对病毒群落分析显示,病毒群落以有尾噬菌体纲(Caudovirales)为主(占74.14%–84.51%),以Lambdavirus和Tequatrovirus为优势。仅1.31%的病毒与已知病毒类群匹配,表明存在大量新病毒。磷富集显著影响病毒群落生态特征,处理组病毒丰度在第35天显著下降,但溶原性比例和病毒生产力未发生显著变化。同时,磷添加导致病毒群落多样性略有降低。值得注意的是,Pepyhexavirus等3个病毒属仅在处理组中检出。病毒-宿主互作预测共获得3,923对关联,覆盖32个宿主属。处理组的病毒-宿主关联数(494对)多于对照组(440对),且Escherichia-Lambdavirus的互作关系在处理组中显著增强。上述结果表明,磷富集选择性重塑了病毒群落,增加了病毒-宿主互作的复杂性。
此外,该研究共鉴定出39个病毒携带的磷代谢相关辅助代谢基因(AMGs-P),主要参与嘧啶、嘌呤和磷酸戊糖代谢。磷富集虽未改变AMGs的整体多样性,但显著影响了其丰度和分布。其中,dut、phoH、thyA、dcd为优势基因,而purL、phnO、pyrE三个基因仅在加磷处理组中检出,分别参与嘌呤/嘧啶代谢和亚磷酸盐利用。这些基因主要源自Siphoviridae等病毒科中的Lambda病毒属等。溯源分析表明,AMGs-P通过水平基因转移来自28个宿主属,以Synechococcus等为主。进一步对phoH基因的系统发育分析显示,该基因广泛分布于病毒、原核和真核生物中,存在频繁的跨物种基因交换。病毒倾向于从宿主中选择性获取特定AMGs(如仅保留两拷贝phoH中的一个),体现了病毒对宿主代谢的精准“盗用”策略,以增强其在磷富集环境下的适应性(图1)。
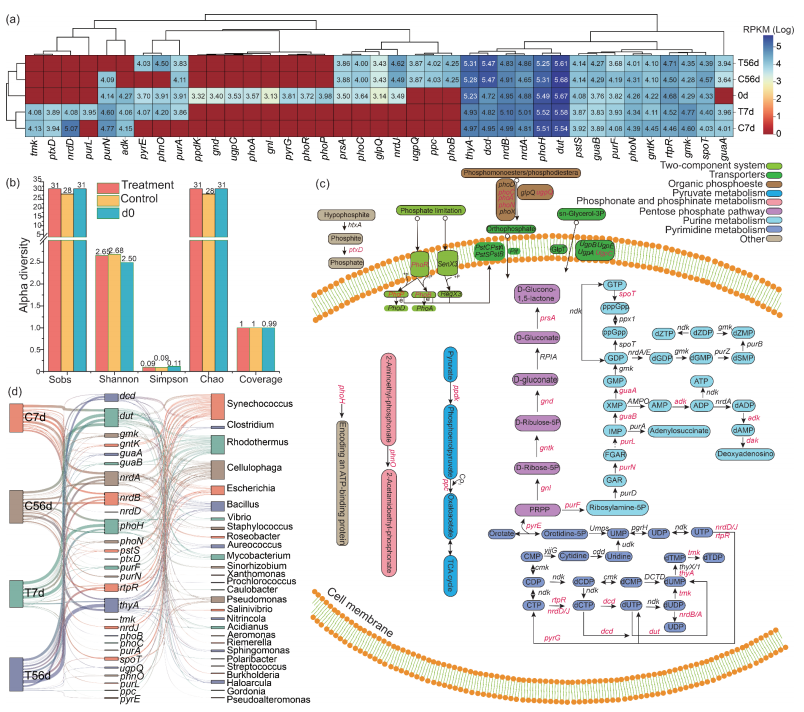
图 1. 与磷相关的病毒辅助代谢基因的丰度、多样性及代谢途径。(a)各组中与磷相关的辅助代谢基因(AMGs-P)的分布情况。(b)AMGs-P 的α多样性。(c)本研究中所鉴定的病毒携带的基因所涉及的磷代谢途径,其中相关基因以红色突出显示。(d)推断的遗传起源关系。
该研究揭示了磷富集条件下病毒群落结构及其代谢功能的响应,证实了磷输入不仅重塑原核微生物群落、促进富营养型类群(如蓝细菌)的扩张,还显著改变病毒群落的β多样性,并富集携带AMGs-P的病毒谱系,从而在磷胁迫下“代谢重塑”宿主功能,加速磷的生物周转。此外,病毒-宿主互作网络在磷富集条件下更加紧密,蓝细菌和α-变形菌成为关键的互作节点,进一步强化了病毒在磷循环中的调控作用。该研究拓展了对病毒作为“代谢调控者”在元素循环中作用的认识,为将病毒过程纳入富营养化预测模型、开发基于AMGs的早期预警指标提供了理论依据和实践参考。
云南大学生命科学学院肖炜副研究员和中国地质大学(武汉)蒋宏忱研究员为论文的共同通讯作者,车绕琼博士生(现就职于云南农业大学)和张仕颖副教授(云南农业大学)为论文的共同第一作者,团队多名老师和同学参与了该项工作。本研究获国家自然科学基金(32071570),云南省农林专项(202301BD070001-110),云南省重点研发计划(202303AP140004)支持。感谢中国科学院抚仙湖高原深水湖泊研究站罗文磊工程师和陈源高教授及云南大学周启超等人对样品采集和实验场地提供的帮助。
原文链接:https://link.springer.com/article/10.1007/s12583-026-0601-6
